状態変化
初めてこれを習うのは、中学生の時の理科だったでしょうか。
初めて習ったときは、普段水以外の物質の状態変化を見ることが無かったので、物質ってみんな状態変化を起こすんだと不思議に思った記憶があります。
そこで今回は、物質の状態変化についてもう一度勉強し直し、分かりやすくまとめてみました!
このページでは、物質の状態変化の他、水での例や温度との関係、沸点・融点についてもお話していますので、ぜひ最後まで読んでみてくださいね(^^)
状態変化とは?
状態変化とは、物質が固体から液体に変化したり、液体から気体に変化したりすることを指す言葉です。
身近なものの例で言えば、水(H2O)が「氷(固体)・水(液体)・水蒸気(気体)」と温度の変化によって姿を変えるのがまさにそうですね。
そして、固体・液体・気体のそれぞれに変化するときの名前も決まっていて、下記のような名前で呼ばれています。
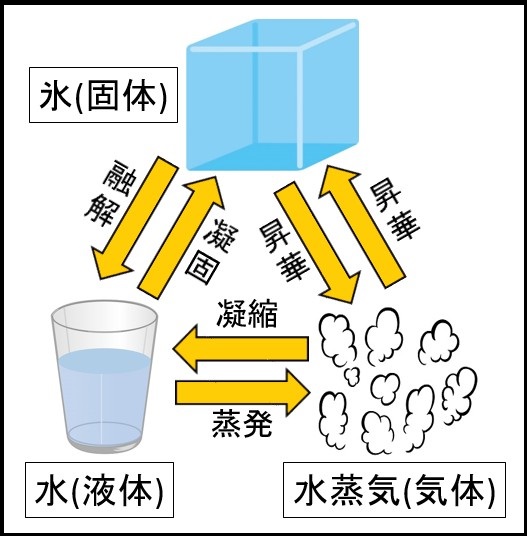
それぞれ、
- 融解=固体から液体への変化
- 凝固=液体から固体への変化
- 蒸発=液体から気体への変化
- 凝縮=気体から液体への変化
- 昇華=固体から気体、または気体から固体への変化
となります。
この中で、なかなかイメージが湧きにくいのは昇華なのではないかと思います。
普段私たちが身近に見ている水では、このようなことは起きませんからね。
そこで、実際の昇華の様子を動画で見てみたいと思います。
この動画では、ヨウ素の昇華現象が分かりやすく撮影されています。
元々固体の状態だったヨウ素がバーナーに熱せらると、固体からすぐに気体に変わってビーカーの中に紫色の気体が充満します。
その後、ビーカーの上に乗っている水の入ったフラスコで冷やされて、そこで結晶となってまた固体の要素に戻ります。
また、身近なところで目にする可能性のある昇華現象としては、ドライアイスの昇華があります。
ドライアイスは地球温暖化の原因物質として有名な二酸化炭素(CO2)が固体になったものですが、常温に置くと液体を経ずにいきなり気体になります。
液体のならないのでこのときにも全くベタベタにならず、これがドライアイスの「ドライ」の名前の由来にもなってます。
ちなみに、ドライアイスを初めて商品化したのはアメリカの「ドライアイス・コーポレーション」という会社で、「ドライアイス」という名称は最初はその会社の商品名でした。
しかし、その商品名がいつの間にか一般化していき、固体の二酸化炭素のことをドライアイスと呼ぶようになりました。
似たような例(商品名の一般化)では、QRコード・ホッチキス・オセロなどがあります。
※固体・液体・気体がそれぞれどのような状態なのかについては別ページで詳しくお話していますので、興味のある方はこちらの記事にも遊びにきてくださいね。
状態変化と温度との関係
ここからは、状態変化と温度との関係を見て行こうと思います。
水が0℃以下になると氷となり、100℃以上になると水蒸気になるように、温度が低いときは固体で、高くなるにつれて液体、気体というふうに変化していきます。
これを図で表すと、下記のグラフのようになります。
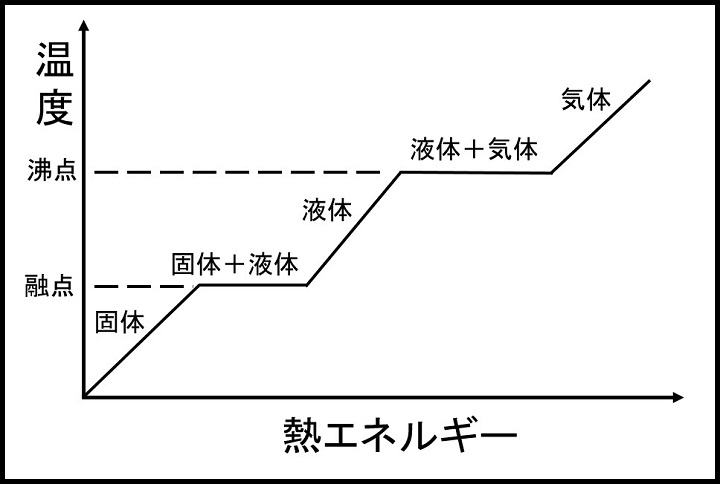
横軸が熱エネルギーの量、縦軸が温度になります。
物質の持っている熱エネルギーの量が少ないと固体、それよりも多くなると液体、さらに多くなると気体へと状態変化が進みます。
融点と沸点
先ほどの表の中のも出てきましたが、固体から液体に変わる時の温度を融点、液体から気体に変わる点を沸点と言います。
そしてもう一つ表の中で注目したい点が、融点と沸点ではグラフが水平になり、熱エネルギーを与えても温度が上がらないという現象が起きます。
例えば水の例でいれば、お鍋に水を入れて火にかけた時、100℃まではどんどん温度が上がっていきますが、100℃になって水の沸騰が始まると、ずっと火にかけたままなのにそれ以上温度が上がらないという現象が起きます。
なぜこのようなことが起こるのかというと、同じ温度でも、固体・液体・気体で持っているエネルギー量が違うからです。
例えば、0℃の氷と0℃の水を比べると、同じ温度ですがエネルギー量は水の方が多く持っています。

そして同じように、100℃の水と100℃の水蒸気を比較すると、100℃の水蒸気のエネルギー量が多いです。
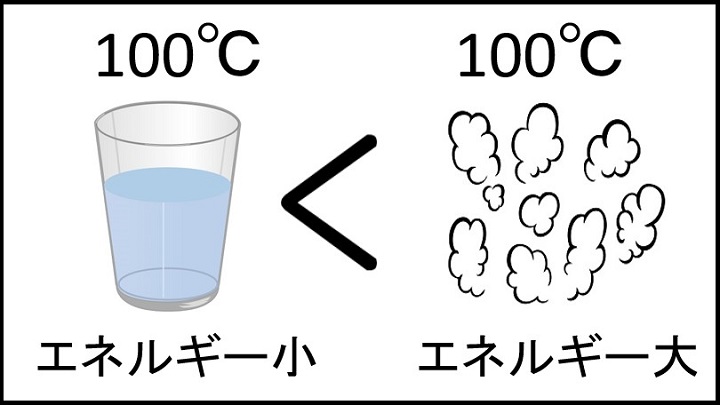
このため、状態変化をするためには、状態が変わるための熱エネルギーを与える必要があります。
このような理由で、状態変化が完了するまではいくら熱エネルギーを与えても温度が変わらないということが起こるのです。
少し難しい言葉になりますが、温度変化に使われる熱を顕熱、状態変化に使われる熱を潜熱と呼びます。状態変化中は熱エネルギーをそのために使うので温度が上がらないので、「潜んだ熱」という意味でこの言葉が使われるようになっています。
※顕熱と潜熱については別ページで詳しくお話していますので、気になる方はこちらも参照されてください。
色々な物質の融点と沸点
最後になりますが、色々な物質の融点と沸点をご紹介したいと思います。
普段我々が目にする状態変化は水がほとんどですが、水以外の物質ももちろん状態変化を起こします。
その融点と沸点をまとめたのがこちらの表です。
| 物質 | ||
|---|---|---|
| 酸素 | ||
| 窒素 | ||
| エタノール | ||
| 水銀 | ||
| 水 | ||
| アルミニウム | ||
| 塩 | ||
| 鉄 |
酸素や窒素などの空気中の成分は融点・沸点がとても低く、普通は気体の状態でしかお目に掛かれませんが、テレビなどで何でも凍らせてしまう液体として使われる液体窒素などは有名ですよね。
また、調味料として大活躍している塩も普段は固体ですが、800℃の高温になると溶けて液体になります。
まとめ
以上で、物質の状態変化についての話を終わります。まとめると、下記の通りです。
- 物質が固体・液体・気体と姿を変えることを状態変化という
- 固体から液体への変化を【融解】という
- 液体から固体への変化を【凝固】という
- 液体から気体への変化を【蒸発】という
- 気体から液体への変化を【凝縮】という
- 固体⇔気体への変化を【昇華】という
- 固体⇔液体へ変化する温度を【融点】という
- 液体⇔気体へ変化する温度を【沸点】という
- 融点・沸点は物質によって違う
- 物質が状態変化をするためには、熱エネルギーが必要
中学生のころはただテストのために覚えるだけだったような気がする状態変化、改めて勉強してみると、とても面白かったです!
これから水などの状態変化を目にする機会があれば、今回勉強したこと思い出しながら見てみると、より楽しくなるかもしれませんね(^^)
編集した本が出版されました!
◆キャリアの話をしよう◆

こちらは、現役管理職ワーママ(部長職)のあづさんが著者の本です。あづさんがインタビューをするという形で、合計4名の女性の方に、ご自身のキャリアをお話しして頂いています。
ここまで等身大のキャリアの話は他では知ることができないと思いますので、キャリアでお悩みの女性の方はぜひ読んでみてください。
◆とろけて香る茄子麻辣のおいしい秘密◆

こちらは、ナス農家をされているハーティッチファーム代表の賀川元史さんが著者の本です。著者さんご自身が開発された日本初の麻婆茄子の瓶詰め「とろけて香る茄子麻辣」の開発秘話です。
いかにして日本初の商品が作られていったのかをストーリー形式でお話ししていますので、ナス好きの方はぜひ読まれてみてください。

























コメントを残す